Rtuť a sloučeniny (jako Hg)
Rtuť a sloučeniny (jako Hg)
- Základní informace
- Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
- H- a P-věty
- Základní charakteristika
- Použití
- Zdroje úniků
- Dopady na životní prostředí
- Dopady na zdraví člověka, rizika
- Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
- Způsoby zjišťování a měření
- Další informace, zajímavosti
- Informační zdroje
Základní informace
| Pořadové číslo látky v IRZ/E-PRTR | 21 |
| Další názvy | sloučeniny rtuti - kalomel, sublimát, fulminát |
| Číslo CAS | 7440-38-2 |
| Chemický vzorec | Hg |
Ohlašovací prahy pro úniky a přenosy pro ohlašování do IRZ/E-PRTR
| Úniky do ovzduší (kg/rok) | 10 |
| Úniky do vody (kg/rok) | 1 |
| Úniky do půdy (kg/rok) | 1 |
| Přenosy v odpadních vodách (kg/rok) | 1 |
| Přenosy v odpadech (kg/rok) | 5 |
| Rizikové složky životního prostředí | ovzduší, voda, půda |
H- a P-věty
| Číslo CAS 7440-38-2; Indexové číslo 080-010-00-X* | |
| Standardní věty o nebezpečnosti | Pokyny pro bezpečné zacházení |
H300 Při požití může způsobit smrt (methylrtuť, dimethylrtuť) H310 Při styku s pokožkou může způsobit smrt (methylrtuť,dimethylrtuť) H331 Toxický při vdechování H314 Způsobuje těžké poleptání kůže a poškození očí (CH3HgCl) H341 Podezření na genetické poškození H350 Může vyvolat rakovinu H360 Může poškodit reprodukční schopnost nebo plod v těle matky H372 Způsobuje poškození orgánů při prodloužené nebo opakované expozici H400 Vysoce toxický pro vodní organismy H410 Vysoce toxický pro vodní organismy, s dlouhodobými účinky | P270 Při používání tohoto výrobku nejezte, nepijte ani nekuřte. P301+P310 Při požití: Okamžitě volejte Toxikologické informační středisko/lékaře /… P330 Vypláchněte ústa. P260 Nevdechujte prach/dým/plyn/mlhu/páry/ aerosoly. P280 Používejte ochranné rukavice/ochranný oděv/ochranné brýle/obličejový štít. P301+P330+P331 Při požití: Vypláchněte ústa. Nevyvolávejte zvracení. P303+P361+P353 Při styku s kůží (nebo s vlasy): Veškeré kontaminované části oděvu okamžitě svlékněte. Opláchněte kůži vodou/osprchujte. P363 Kontaminovaný oděv před opětovným použitím vyperte. P304+P340 Při vdechnutí: Přeneste osobu na čerstvý vzduch a ponechte ji v poloze usnadňující dýchání. P310 Okamžitě volejte Toxikologické informační středisko/lékaře/… P305+P351+P338 Při zasažení očí: Několik minut opatrně vyplachujte vodou. Vyjměte kontaktní čočky, jsou-li nasazeny, a pokud je lze vyjmout snadno. Pokračujte ve vyplachování. P201 Před použitím si obstarejte speciální instrukce. P202 Nepoužívejte, dokud jste si nepřečetli všechny bezpečnostní pokyny a neporozuměli jim. P308+P313 Při expozici nebo podezření na ni: Vyhledejte lékařskou pomoc/ošetření. P314 Necítíte-li se dobře, vyhledejte lékařskou pomoc/ošetření. P273 Zabraňte uvolnění do životního prostředí. P391 Uniklý produkt seberte. |
* Indexové číslo, harmonizovaná klasifikace dle přílohy VI, nařízení (ES) č. 1272/2008, ve znění pozdějších předpisů.
Základní charakteristika
Chemický prvek rtuť je stříbrobílý, velmi lesklý kov, v tuhém stavu krystalizuje v trigonální nebo hexagonální soustavě. Unikátní vlastnosti rtuti jsou známé již od starověku. Je to za normálních podmínek jediný kapalný kov, který má jako kapalina naprosto neobvyklou, extrémně vysokou hustotu (13,5 g.ml-1) a nezanedbatelnou těkavost (tense par je 0,3 Pa při 25 °C). Pro alchymisty měla rtuť přímo mystický význam. Je poměrně špatným vodičem tepla, ale dobrým elektrickým vodičem. Rtuť snadno tvoří slitiny (amalgámy) skoro se všemi běžnými kovy, včetně stříbra, hliníku a zlata. Se železem však slitinu netvoří. Běžným oxidačním stavem je +1 a +2, výjimečně se vyskytuje ve stavu 3+.
Použití
Na evropské úrovni již dlouhodobě platí více než 40 právních předpisů (nařízení, směrnice), jejichž cílem je minimalizovat používání rtuti a snížit tak rizika spojená s negativními účinky rtuti na člověka a životní prostředí. Omezování použití rtuti v celé EU se týká např. dovozu kovové rtuti, omezení vývozu výrobků obsahujících rtuť (teploměry, měřící techniky,..), omezení použití rtuti v určitých výrobních procesech a u nových výrob a výrobků, zákaz těžby zlata v malém měřítku pomocí rtuti a omezení použití dentálního amalgámu (zatím jen zákaz amalgámových plomb pro děti a těhotné či kojící ženy). I když je používání rtuti omezeno i v chemických laboratořích, nelze se mu zcela vyhnout. Přinejmenším v polarografii a v některých dalších elektrochemických aplikacích je nepostradatelná. Aromatické sloučeniny rtuti obsahující arylhydrargyriové kationty se používali jako pesticidy v zemědělství a jako meziprodukty v organické syntéze. Tyto látky pomalu uvolňují elementární rtuť reakcí, která se v organokovové chemii nazývá reduktivní eliminace. Rtuť se používá primárně na výrobu průmyslových chemikálií, v elektronice a elektrotechnice. Malé elektrické články obsahující rtuť se často používají např. v naslouchacích přístrojích, kamerách, hračkách, malých přenosných radiopřijímačích, kalkulačkách, měřících přístrojích, detektorech kouře a radiomikrofonech. Svítidla s obsahem rtuti (zářivky, rtuťové lampy) mají vyšší světelnou účinnost než klasické žárovky s wolframovým vláknem. Používají se pro vnitřní i vnější osvětlení, v promítacích přístrojích a v reflektorech, ve zdravotnictví, laboratořích, při fotografování apod. Elementární rtuť se v minulosti používala jako náplň teploměrů a tlakoměrů na měření atmosférického tlaku. Dobré elektrické vodivosti rtuti se občas využívá ke konstrukci sklopných spínačů elektrického proudu.
Značné použití má rtuť také při výrobě amalgámů, např. dentálního amalgámu. Tvorby amalgámu se zlatem se běžně využívalo při těžbě zlata z rud o vysoké kovnatosti. Bohužel velká množství rtuti se dodnes používají při řemeslném způsobu těžby zlata v chudých zemích Afriky a jihovýchodní Asie. Tato těžba představuje v současnosti hlavní a největší zdroj zamoření ekosystémů rtutí a má katastrofální následky na zdraví místních obyvatel. Sodíkový amalgám vzniká při elektrolýze chloridu sodného s použitím rtuťové katody a dále se používá k výrobě hydroxidu sodného a plynného chloru. Rtuť se používá také jako katalyzátor při výrobě uretanové pěny a antrachinonu. Některé léky (diuretika, antiseptika, dermatologika) obsahují rtuť nebo její sloučeniny. Bývá obsažena jako antibakteriální a fungicidní přísada v nátěrových hmotách, vyskytuje se i v mazacích olejích. Rtuť nalézá uplatnění v analytické chemii. V polarografii se využívá rtuťová elektroda, často používanou referenční elektrodou je kalomelová elektroda (z chloridu rtuťného). Další uplatnění nalézá kalomel v gravimetrické analýze platinových kovů, kde působí jako selektivní redukční činidlo. Chlorid rtuťnatý (sublimát) byl dříve používán jako součást jedů na hlodavce a k moření obilí. Fulminát rtuťnatý (azid rtuti) je znám jako třaskavá rtuť. Tato sloučenina slouží k výrobě pyrotechnických rozbušek. Až do počátku 20. století se rtuťové přípravky hojně používaly i v léčbě různých nemocí. Např. lékař a alchymista Paracelsus (1492-1541) s úspěchem používal rtuť při léčbě syfilidy, nemoci, která se v té době rychle šířila Evropou a se kterou si lékaři nevěděli rady. Podobné preparáty obsahující rtuť se používaly jako relativně nejúčinnější prostředky k léčbě této nemoci až do objevu Salvarsanu v 19. století.
Zdroje úniků
Většina emisí rtuti je antropogenního původu. Přibližně 80 % rtuti uvolňované lidskou činností je emitováno do vzduchu ve formě kovové rtuti. Primárním zdrojem je spalování fosilních paliv a odpadů. Významné jsou emise způsobené těžbou a zpracováním rud s obsahem rtuti. Zhruba 15 % celkových emisí rtuti se dostává do půdy z hnojiv, fungicidů, komunálního odpadu a atmosférickou depozicí. Zbývajících 5 % je uvolňováno do vody prostřednictvím průmyslových odpadních vod. Přirozenými zdroji rtuti v prostředí je zvětrávání přírodních ložisek a sopečné výbuchy. Průmysl zvyšuje globální znečištění rtutí především výrobou chlóru a alkalických hydroxidů pomocí amalgámové elektrolýzy a těžbou zlata amalgámovou technologií.
Mezi nejvýznamnější antropogenní zdroje rtuti patří:
- Spalování fosilních paliv a odpadu;
- Emise spojené s těžbou a zpracováním rud s obsahem rtuti;
- Používání hnojiv a fungicidů s obsahem rtuti.
Dopady na životní prostředí
Většina rtuti v prostředí se vyskytuje ve formě kovové rtuti nebo anorganických sloučenin. Kovová rtuť je za normálních podmínek kapalná, dochází však k částečnému odpařování. Ve vzduchu může docházet k přeměnám na jiné formy a rtuť může být transportována na velké vzdálenosti. Některé mikroorganismy (bakterie, fytoplankton, plísně) mohou přeměňovat anorganickou rtuť na organické sloučeniny. Rtuť setrvává v prostředí po dlouhou dobu, zvláště pokud je navázána na malé půdní částice. Tyto částice obvykle zůstávají na povrchu sedimentů a půd a nepřecházejí do podzemních vod. Ve vodním prostředí se usazují na dně. Organická rtuť se může hromadit v potravních řetězcích, zatímco anorganická rtuť do potravních řetězců nevstupuje. Popsanou vlastnost lze nazývat bioakumulací. Nejvyšší obsahy organické rtuti v těle se nacházejí u mořských ryb, vysoké koncentrace rtuti mohou obsahovat i houby. Naopak, akumulace v rostlinách není příliš vysoká.
Dopady na zdraví člověka, rizika
Rtuť je typickým zástupcem neurotoxických kovů. Toxicita jednotlivých sloučenin rtuti je závislá především na jejich rozpustnosti ve vodě. Z tohoto pohledu jsou nejvíce rizikové sloučeniny dvojmocné rtuti Hg2+. Naopak toxicita samotné elementární (kovové) rtuti je prakticky nulová, protože jen obtížně vniká do organických tkání, při perorálním vstupu má velmi malou biologickou dosažitelnost - ze zažívacího traktu se vstřebává méně než 0,1 % dávky. Mnohem škodlivější jsou její páry, které při běžné teplotě místnosti mohou vytvořit koncentrace přesahující hygienické limity (PEL je 0,002 mg m-3). Páry rtuti jsou sedmkrát těžší než vzduch a proto se mohou hromadit v špatně odvětrávaných níže položených oblastech. Kovová rtuť se dostává přes hematoencefalickou barieru (ale i placentu) z krve přes plíce do mozku a narušuje nervovou komunikaci. Nejohroženější skupinou jsou kojenci a nenarozené děti. Chronické otravy anorganickými sloučeninami rtuti jsou známé pod označením merkurialismus a projevují se jemným třesem končetin a změnami chování. Oběti jsou náladové, často předrážděné, mají sklony k agresivním reakcím, pocity sebevědomí střídají depresivní stavy. Často dochází k poškození nebo až k selhání ledvin.
Zvláště nebezpečné jsou organokovové sloučeniny rtuti, které se mohou snadno dostat do živých tkání a to například i pouhým stykem s pokožkou. Tyto sloučeniny se dostávají do životního prostředí např. rozkladem různých organických sloučenin s obsahem rtuti nebo i metabolickými pochody mikroorganismů při styku se rtutí. Nejčastěji uváděným příkladem je dimethylrtuť (kapalná látka), u které je jako smrtelná dávka pro dospělého člověka uváděno množství pouze 0,1 ml.
Z potravin jsou rizikovým faktorem z hlediska obsahu rtuti především vnitřnosti (játra, ledviny) nebo ryby, které byly kontaminovány rtutí při svém růstu. Rizikové mohou být i zemědělské plodiny, pěstované na půdě zamořené rtuťnatými sloučeninami ať již z průmyslových zdrojů nebo nevhodně použitými přípravky k hubení zemědělských škůdců.
Rtuť patří mezi prvky, jejichž vliv na zdravotní stav lidského organismu je jednoznačně negativní. Je kumulativním jedem, z organismu se vylučuje jen velmi pozvolna. Koncentruje se především v ledvinách a v menší míře i v játrech a slezině. V ledvinách může setrvat až desítky let. Právě ty jsou při chronické otravě rtutí nejvíce ohroženy. Projevy chronické otravy bývají často nespecifické - od studených končetin, vypadávání vlasů, přes zažívací poruchy, různé neurologické a psychické potíže až po závažné stavy jako např. chudokrevnost, revmatické choroby či poškození ledvin. Chronická expozice také může způsobovat vypadávání zubů, vyrážky, svalový třes, ztrátu paměti, změny v chování a poškození mozku a centrální nervové soustavy. Při jednorázové vysoké dávce rtuti se dostavují bolesti břicha, průjmy a zvracení. Akutní expozice parám rtuti může způsobit zánět plic, poškození ledvin a zvýšení krevního tlaku. Rtuť může mít také vliv na plodnost. Organické sloučeniny rtuti způsobují poškození mozku a nervové soustavy. Nejnebezpečnější známou sloučeninou rtuti je Dimethylrtuť (správněji nazývaná dimethylhydrargyrium Me2Hg), která byla příčinou četných otrav u lidí, kteří s ní pracovali. Známý se stal tragický případ profesorky K. Wetterhahnové - když pipetovala dimethylrtuť, malé množství ji ukáplo na ruku chráněnou latexovou rukavicí. Asi po pěti měsících si všimla charakteristických příznaků otravy – zúžení zorného pole, brnění prstů rukou i nohou a problémů s rovnováhou. Krátce nato upadla do kómatu a asi devět měsíců po intoxikaci zemřela. Dimethylrtuť totiž snadno proniká latexovou rukavicí i kůží a rychle se absorbuje. Také methylrtuť byla příčinou několika doložených hromadných otrav. Nejhorší následky měla otrava mořeným obilí v Iráku v zimě 1971-72 následující po roce neúrody. Tehdy Iráčané semleli a snědli mořené osivo. Otrava si vyžádala více než 6 000 obětí na lidských životech (WHO 1990). Ještě známější je případ hromadné otravy v japonské Minamatě. Místní chemická továrna Chisso vypouštěla do moře zbytky rtuťnatých solí používaných jako katalyzátor. V moři se anorganická rtuť působením mikroorganismů přeměňovala na methylrtuť a potravním řetězcem přes ryby se dostala až do těl místních rybářů a domácích zvířat. Nejprve obyvatelé pozorovali podivné chování koček, které se vrhaly střemhlav do moře. Později se příznaky otravy začaly projevovat i u lidí a dostaly jméno minamatská nemoc. Projevovala se různým stupněm postižení nervového systému s příznaky podobnými jako u výše popsané otravy dimethylrtuti. Podle oficiálních záznamů si tato hromadná otrava za 36 let vyžádala 1043 obětí z celkového počtu nemocných přesahujícího 2 tisíce. Nejohroženější skupinou jsou kojenci a nenarozené děti Příznaky chronické otravy zahrnují poruchy řeči, sluchu, chůze a periferního vidění, narušení koordinace pohybů, třes rukou, emoční nestabilitu (vznětlivost, únavu, poruchy spánku), záněty dásní a svalovou slabost. Kationty rtuti jsou měkkými elektrofily a tvoří proto velmi pevné vazby se sírou. Struktura proteinů je pak narušena stabilními metalosulfidickými můstky (-S-Hg-S-).
V České republice platí pro koncentrace rtuti a jejích sloučenin následující limity v ovzduší pracovišť:
- pro rtuť: PEL – 0,05 mg.m-3, NPK - P – 0,15 mg.m-3;
- pro alkylsloučeniny rtuti: PEL – 0,01 mg.m-3, NPK - P – 0,03 mg.m-3.
- pro anorganické a arylsloučeniny rtuti: PEL – 0,05 mg.m-3, NPK - P – 0,15 mg.m-3.
Celkové zhodnocení nebezpečnosti z hlediska životního prostředí
Rtuť je jeden z nejtoxičtějších prvků. Vyskytuje se ve všech složkách životního prostředí. Anorganické sloučeniny rtuti se mohou v anaerobním prostředí vlivem činností mikroorganismů přeměňovat na organické, které se mohou hromadit v potravním řetězci. Organické sloučeniny rtuti jsou toxičtější než anorganické, tyto látky se z organismu prakticky nevylučují.
Způsoby zjišťování a měření
Množství vypouštěné rtuti je možné odhadnout z rozdílu mezi koncentrací rtuti v surovině a v produktu. Ke stanovení obsahu rtuti lze využít tzv. techniku studených par rtuti, což je speciální provedení metody atomové absorpční spektrometrie využívající vypařování rtuti. Měření mohou provést komerční laboratoře nebo se lze obrátit na specializovaná pracoviště (např. centrální laboratoře atomové spektrometrie VŠCHT Praha). Pro stanovení rtuti v matricích je k dispozici řada normovaných postupů:
| Norma | Metoda měření | Oblast použití |
| EN 14385:2004 | Stanovení celkových emisí Hg, As, Cd, Cr, Co, Cu, Mn, Ni, Pb, Sb, TI a V | Kvalita ovzduší, emise ze stacionárních zdrojů |
| EN 14884:2005 | Atomová absorpční spektrometrická metoda (bezplamenová s amalgamací: AMA 254) (ISO 11969:1996) | Kvalita ovzduší |
| EN ISO 11969:1996 | Stanovení celkového As spektrofotometrickou metodou s diethyldithiokarbamanem stříbrným (ISO 6595:1982) | Kvalita vod |
Ohlašovací práh pro emise do vody je dosažen například při vypouštění 1 000 m3 odpadní vody o koncentraci rtuti 1 mg.l-1. Práh pro emise do ovzduší je dosažen například při vypouštění 1 000 000 m3 odpadního vzduchu o koncentraci 10 mg.m-3.
Další informace, zajímavosti
V běžném životě se se rtutí nejčastěji setkáváme v podobě dentálního amalgámu, který se používá v zubním lékařství jako velmi odolná výplň zubu po odstranění zubního kazu. V současné době se používají amalgámy, které vzniknou smísením rtuti se slitinou stříbra, mědi a cínu. Poměr posledních tří prvků se liší podle jednotlivých výrobců a obchodních značek. Dentální amalgám musí splňovat řadu přísných kritérií. Rychlost tuhnutí musí být taková, aby lékař měl dostatek času plombu do zubu správně zasadit a mechanicky upravit, současně by však již po hodině až dvou měla být natolik tvrdá, že ji pacient může používat. Během tvrdnutí nesmí docházet k velkým rozměrovým změnám amalgámu – při expanzi by hrozilo roztržení zubu, při zmenšení objemu by plomba vypadávala. Amalgám musí být co nejvíce chemicky odolný vůči prostředí v lidských ústech, aby nedocházelo k uvolňování rtuti a zbylých kovů do organismu. Přestože se v současné době používá amalgám v dentální medicíně stále méně a je nahrazován různými plastickými polymery, jsou jeho mechanické vlastnosti stále nejlepší ze všech zubních výplní. Používá se především k výplním stoliček, kde nevadí jeho tmavá barva, ale plně se uplatní tvrdost a dlouhodobá mechanická odolnost. Od 1. července 2018 platí, až na výjimky, zákaz používání amalgámových plomb u dětí do patnácti let, těhotných a kojících žen. Místo amalgámu jim pojišťovny hradí takzvaný skloionomerní cement. Nové předpisy omezující používání rtuti souvisí s její škodlivostí lidskému zdraví i životnímu prostředí. Evropský parlament je schválil již v roce 2017.
Obrázek 1 ukazuje vztahy mezi koncentrací rtuti a možným ohrožením. Graf je k dispozici na webových stránkách agentury US EPA (USA).
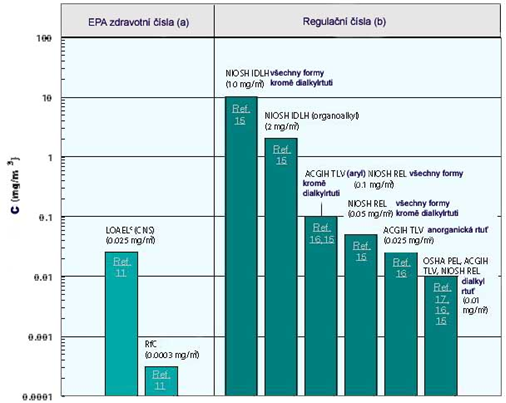
Obrázek 1: Vztahy mezi koncentrací rtuti a možným zdravotním rizikem
Informační zdroje
- Encyklopedie Wikipedia, https://cs.wikipedia.org/wiki/Rtu%C5%A5, https://en.wikipedia.org/wiki/Mercury_(element)
- Agency for Toxic Substances and Disease Registry, https://www.atsdr.cdc.gov
- Environment Agency, https://www.gov.uk/government/organisations/environment-agency
- PubChem, Open Chemistry Database, https://pubchem.ncbi.nlm.nih.gov/compound/23931
- Centers for Disease Control and Prevention, https://www.cdc.gov/niosh/topics/mercury/
- US EPA IRIS, https://cfpub.epa.gov/ncea/iris2/chemicalLanding.cfm?substance_nmbr=370
- Databáze Eurochem, https://chemax.cz/#/record/eTE2VlM1L2NZaXc9
- Harte J., Holdren C., Schneider R., Shirley Ch.: Toxics A to Z, A Guide to Everyday Pollution Hazards, University of California Press, 1991
- Weiner E. R.: Applications of Environmental Chemistry, A Practical Guide for Environmental Professionals, Lewis Publishers, 2000
- Horáková M.: Analytika vody, VŠCHT Praha, 2003
- Pitter P.: Hydrochemie, Vydavatelství VŠCHT, 1999
- Paleček J., Linhart I., Horák J.: Toxikologie a bezpečnost práce v chemii, VŠCHT Praha 2008
- Miroslav Šuta: REACH: 14 nebezpečných chemických látek přidáno na „černou listinu“, respekt.cz, 24. ledna 2010
- Periodická tabulka, http://www.prvky.com/80.html
- Evropský parlament, http://www.europarl.europa.eu/sides/getDoc.do?pubRef=-//EP//TEXT+IM-PRESS+20070706IPR08897+0+DOC+XML+V0//CS
- Linhart J: Toxikologie, VŠCHT Praha, 2014
- Encyklopedie Britannica, https://www.britannica.com/science/mercury-chemical-element
- European Industrial Emissions Portal, https://industry.eea.europa.eu/pollutants/pollutant-index
- ČSN online, https://csnonline.agentura-cas.cz/
- Right to Know Hazardous Substance Fact Sheets, State of New Jersey Department of Health, https://web.doh.state.nj.us/rtkhsfs/indexfs.aspx